 |
Главная |
Свойства пиррола и его производных
|
из
5.00
|
Пиррол проявляет крайне слабые основные свойства при взаимодействии с концентрированными минеральными кислотами (см. ацидофобность пиррола). За счёт полярности NH-связи проявляются слабые кислотные свойства. Пиррол образует соли при взаимодействии с щелочными металлами или их амидами:
 |
Даже вода, являясь более сильной кислотой, чем пиррол, вытесняет его из солей.
Реакции восстановления (гидрирования) пиррола протекают в довольно жёстких условиях, ступенчато:
 |
 Пирролидин – сильное основание (как вторичный алифатический амин). Ядро пирролидина входит в структуру алкалоида никотина, аминокислоты пролина:
Пирролидин – сильное основание (как вторичный алифатический амин). Ядро пирролидина входит в структуру алкалоида никотина, аминокислоты пролина:
 |
 Важную группу азотсодержащих природных веществ составляют так называемые тетрапиррольные соединения, т.е. соединения, в структуру которых входят четыре пиррольных кольца. К тетрапиррольным соединениям относится порфин, производными которого являются такие биологически важные соединения как хлорофилл, гем, цитохром. Порфин является устойчивой ароматической системой (энергия сопряжения – 840 кДж/моль). В замкнутой p,π-сопряженной системе делокализовано 26 электронов.
Важную группу азотсодержащих природных веществ составляют так называемые тетрапиррольные соединения, т.е. соединения, в структуру которых входят четыре пиррольных кольца. К тетрапиррольным соединениям относится порфин, производными которого являются такие биологически важные соединения как хлорофилл, гем, цитохром. Порфин является устойчивой ароматической системой (энергия сопряжения – 840 кДж/моль). В замкнутой p,π-сопряженной системе делокализовано 26 электронов.
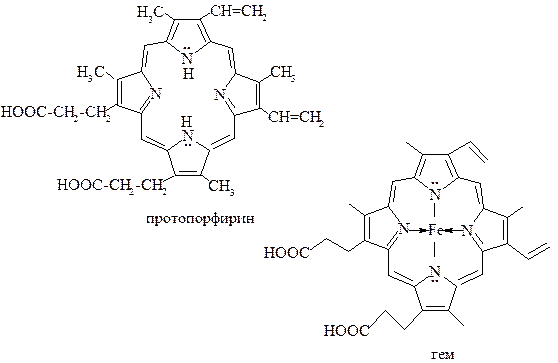 Порфины, имеющие заместители в пиррольных циклах, называются порфиринами. Заместители могут содержать кратные связи, способные вступать в сопряжение с ароматическим облаком, что еще более стабилизирует молекулу. Пример порфирина – протопорфирин, входящий в структуру гемоглобина крови.
Порфины, имеющие заместители в пиррольных циклах, называются порфиринами. Заместители могут содержать кратные связи, способные вступать в сопряжение с ароматическим облаком, что еще более стабилизирует молекулу. Пример порфирина – протопорфирин, входящий в структуру гемоглобина крови.
Порфирины находятся в природе в виде комплексов с металлами. Комплекс порфирина с железом – гем – небелковая часть молекулы гемоглобина и цитохромов. Комплекс с магнием является основой молекулы хлорофилла.
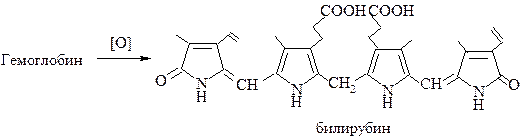 При биологическом окислении гемоглобина образуются окрашенные вещества с линейной тетрапиррольной структурой – билирубиноиды, например, билирубин, имеющий оранжевую окраску.
При биологическом окислении гемоглобина образуются окрашенные вещества с линейной тетрапиррольной структурой – билирубиноиды, например, билирубин, имеющий оранжевую окраску.
 Индол (бензопиррол) – конденсированное гетероциклическое соединение. В его молекуле сконденсированы бензольное и пиррольное кольца. Индол ароматичен. В его p,π-сопряженной системе делокализовано 10 электронов.
Индол (бензопиррол) – конденсированное гетероциклическое соединение. В его молекуле сконденсированы бензольное и пиррольное кольца. Индол ароматичен. В его p,π-сопряженной системе делокализовано 10 электронов.
 По свойствам индол подобен пирролу. Его основные свойства практически не проявляются, он ацидофобен, обладает слабыми NH-кислотными свойствами. Индол вступает в реакции электрофильного замещения легче, чем бензол. Реакции SE протекают по β-положению пиррольного кольца:
По свойствам индол подобен пирролу. Его основные свойства практически не проявляются, он ацидофобен, обладает слабыми NH-кислотными свойствами. Индол вступает в реакции электрофильного замещения легче, чем бензол. Реакции SE протекают по β-положению пиррольного кольца:
Наиболее важными биологически активными производными индола являются α-аминокислота триптофан и продукты его метаболических превращений.
 Триптофан входит в структуру белков. В организме он подвергается метаболическим превращениям по двум направлениям: неокислительное и окислительное декарбоксилирование:
Триптофан входит в структуру белков. В организме он подвергается метаболическим превращениям по двум направлениям: неокислительное и окислительное декарбоксилирование:
В результате неокислительного декарбоксилирования образуется токсичный биогенный амин триптамин, который затем подвергается дальнейшему превращению в β-индолилуксусную кислоту.
При окислительном декарбоксилировании вначале образуется 5-гидрокситриптофан, который затем декарбоксилируется в 5-гидрокситриптамин (серотонин). Серотонин является одним из нейромедиаторов головного мозга. Нарушение его нормального обмена в организме может привести к шизофрении. В норме серотонин окисляется в (5-гидрокси-β-индолил)уксусную кислоту и выводится с мочой.
 Другим важным производным индола является нестероидный противовоспалительный препарат индометацин.
Другим важным производным индола является нестероидный противовоспалительный препарат индометацин.
|
из
5.00
|
Обсуждение в статье: Свойства пиррола и его производных |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

