 |
Главная |
Правила определения степени окисления
|
из
5.00
|
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
ТЕОРЕТИЧЕСКОЕ ВВЕДЕНИЕ
Окислительно-восстановительные реакции – это реакции, протекающие с изменением степени окисления.
Степень окисления (СтО) – это условный заряд атома в молекуле, вычисленный исходя из предположения, что молекула состоит только из ионов.
Степень окисления может быть положительной, отрицательной или нулевой. Атомы одного и того же элемента в разных соединениях проявляют различные степени окисления.
Степень окисления показывает, сколько электронов смещено от атома данного элемента (положительная степень окисления) или к атому данного элемента (отрицательная степень окисления). Смещение электронов происходит к наиболее электроотрицательному элементу.
Нулевую степень окисления имеют атомы в молекулах простых веществ (образованных атомами одного элемента). В них элементы имеют абсолютно одинаковые электроотрицательности и электроны не смещаются ни к одному из атомов.
Правила определения степени окисления
1. Существуют элементы, проявляющие во всех молекулах сложных веществ постоянную степень окисления:
– Элементы І группы главной подгруппы (щелочные металлы): Li+, Na+, K+, Rb+, Cs+, а также Ag+;
– Водород Н+ (кроме гидридов металлов  )
)
– Элементы ІІ группы главной подгруппы (щелочно-земельные металлы): Be+2, Mg+2, Ca+2, Sr+2, Ba+2; а также Zn+2;
–Элементы ІІІ группы главной подгруппы: B+3, Al+3;
– Кислород О-2, кроме пероксидов (  ,
, 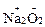 ,
,  ), надпероксидов
), надпероксидов  , озонидов
, озонидов 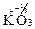 и фторида кислорода
и фторида кислорода  .
.
2. Высшая степень окисления элемента равна номеру группы элемента (N) в таблице Менделеева. СтОmax = N:
Cl+7(VII гр.), S+6(VI гр.), N+5(V гр.), Mn+7(VII гр.), Cu+2(II гр.).
Низшая степень окисления элемента равна: СтОmin = N – 8:
Cl–(VII гр.), S–2(VI гр.), N–3(V гр.), C–4(IV гр.).
3. Степени окисления элементов в сложных веществах определяются, исходя из правила: сумма степеней окисления всех атомов в молекуле равна нулю, в ионе – заряду иона.
Пример: В молекуле дихромата калия K2Cr2O7 степени окисления калия и кислорода постоянны: К+, О‑2; степень окисления хрома является переменной, ее необходимо определить.
Так как сумма всех степеней окисления в молекуле равна нулю, можно составить уравнение, обозначив степень окисления хрома за х:
2(+1) + 2х + 7(-2) = 0,
откуда х = 6.
Степень окисления хрома равна +6: 
Окисление – процесс отдачи электронов атомом, молекулой или ионом.
Частицы, отдающие электроны – восстановители.
В процессе окисления степень окисления восстановителя повышается.
Восстановление – процесс присоединения электронов атомом, молекулой или ионом.
Частицы, принимающие электроны – окислители.
В процессе восстановления степень окисления окислителя понижается.
Процесс передачи электронов от восстановителя к окислителю подчиняется правилу электронного баланса:число электронов отданных восстановителем всегда равно числу электронов принятых окислителем.
Существует два метода составления уравнений окислительно-восстановительных реакций: метод электронного баланса и метод полуреакций (ионно-электронный метод).
|
из
5.00
|
Обсуждение в статье: Правила определения степени окисления |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

