 |
Главная |
Расчеты по уравнениям химических реакций
|
из
5.00
|
Для необратимой химической реакции, определяемой стехиометрическим уравнением
νАА + νВВ + … = νСС + νDD + …
формульные количества веществ (вступивших в реакцию реагентов и образовавшихся продуктов) nA, nB, … , nC, nD, … , пропорциональны соответствующим стехиометрическим коэффициентам:
 =
= 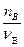 = … =
= … =  =
=  = …
= …
Если формульное количество одного из веществ (реагента или продукта) задано условием задачи, то вышеприведенное выражение позволяет рассчитать формульные количества (а следовательно, массы и объемы) участвующих в данной реакции всех остальных веществ в соответствии с ее стехиометрией.
Практическое решение типовой химической задачи складывается из нескольких этапов:
а) в соответствии с текстом задачи составляется уравнение реакции, а затем необходимые для расчета формулы веществ обозначаются буквами А, В, С, D, … (для одноатомных простых веществ используются непосредственно символы соответствующих элементов);
б) записывается краткое условие задачи; вначале указывают искомую величину, а затем заданную величину (или величины); все буквенные обозначения величин сопровождаются (в нижнем индексе) указанием, к каким веществам они относятся, например, mA, nB, MC, VD, mNa, nAl, MS, VAr; для каждой заданной величины приводят ее значение по условию;
в) составляется (выводится) математическая формула для искомой величины, выраженной только через заданные величины и необходимые константы; проводится проверка расчетной формулы на соответствие единиц (при необходимости делается корректировка единиц в условии задачи);
г) условие задачи дополняется теми константами, которые вошли в расчетную формулу; при этом необходимые для решения табличные данные берутся из таблиц Приложения;
д) числовые значения величин подставляются в расчетную формулу, выполняется расчет значения искомой величины, указывается единица искомой величины;
е) записывается подробный ответ задачи.
Пример 1. Определите формульное количество вещества (моль) в оксиде хрома (III), затраченном на получение 21,4 г диоксохромата (III) натрия по реакции
Cr2O3 + Na2CO3  2NaCrO2 + CO2
2NaCrO2 + CO2
 Рассчитайте также объем (л, н. у.) выделившегося газа.
Рассчитайте также объем (л, н. у.) выделившегося газа.
Решение
nA = ? Cr2O3 + Na2CO3  2NaCrO2 + CO2
2NaCrO2 + CO2
VC = ? (A) (B) (C)
mB = 21,4 г
 nA =
nA =  =
=  =
=  = 0,1 моль;
= 0,1 моль;
νА = 1
νВ = 2 VC = VM∙nC = 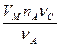 =
=  = 2,24 л.
= 2,24 л.
MB = 106,98 г/моль
VM = 2
VC = 1
Ответ. В данной реакции участвует 0,1 моль Cr2O3 и образуется 2,24 л CO2.
Пример 2. Рассчитайте объем (мл) воды, необходимый для проведения реакции
Al4C3 + 12H2O = 4Al(OH)2  + 3CH4
+ 3CH4 
если имеется 99,85 г трикарбида тетраалюминия. Плотность воды принять равной 0,9982 г/мл.
 Решение
Решение
VB =? Al4C3 + 12H2O = 4Al(OH)2  + 3CH4
+ 3CH4 
mA = 99,85 г (A) (B)
ρB = 0,9982 г/мл
 VB =
VB =  =
=  =
=  =
=  =
=  =
=
MB = 18,02 г/моль =150,25 мл
νВ = 12
νА = 1
МА = 143,96 г/моль
Ответ. Для проведения данной реакции надо взять 150,25 мл Н2О.
Пример 3. К 100 мл 0,05 М раствора Al2(SO4)3 добавляют 0,25 М раствор NH3∙H2O до полного выпадения осадка гидроксида алюминия. Какой объем (мл) раствора гидрата аммиака затрачен на реакцию?
Решение
 V(p)B =? Al2(SO4)3 + 6(NH3∙H2O) = 2Al(OH)3
V(p)B =? Al2(SO4)3 + 6(NH3∙H2O) = 2Al(OH)3  + 3(NH4)2SO4
+ 3(NH4)2SO4
V(p)A = 100 мл (A) (B)
cA = 0,05 моль/л
cB = 0,25 моль/л
 V(p)B =
V(p)B =  =
=  =
=  =
= 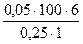 = 120 мл
= 120 мл
νВ = 6
νА = 1
Ответ. На проведение реакции затрачено 120 мл раствора NH3∙H2O.
|
из
5.00
|
Обсуждение в статье: Расчеты по уравнениям химических реакций |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

