 |
Главная |
IV этап: выход продуктов из области активного центра фермента.)
|
из
5.00
|
Кинетика ферментативных реакций.
I. Зависимость скорости реакции от концентрации субстрата:
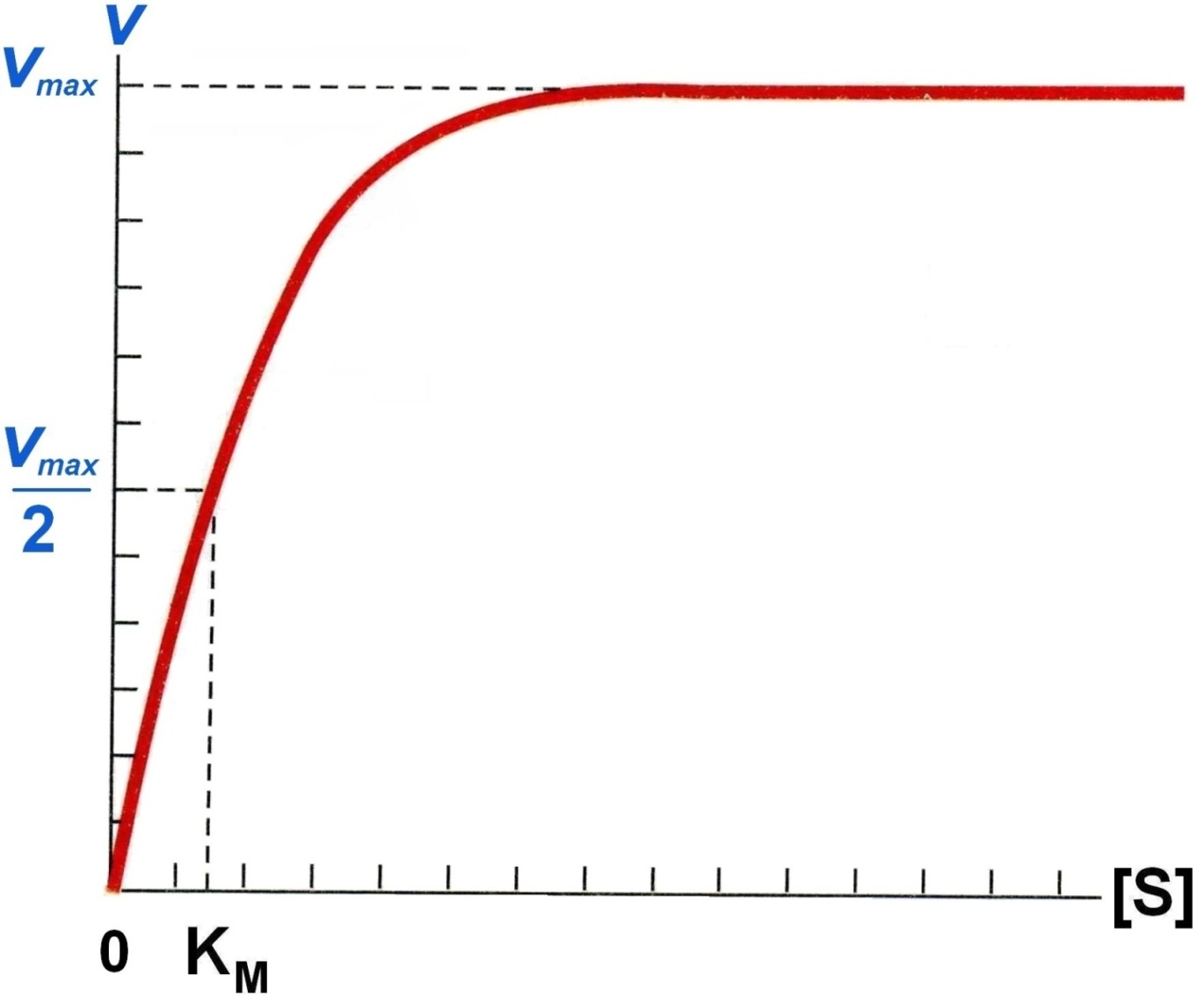
Vmax – это такая V ферментативной реакции, при которой достигается полное насыщение фермента субстратом, т.е. когда все активные центры фермента связаны с субстратом.
KM – константа Михаэлиса:
1) KM численно равна концентрации субстрата, при которой скорость реакции равна ½ Vmax.
2) KM показывает сродство E к S. Чем меньше KM, тем больше сродство и наоборот.
II. Зависимость скорости реакции от температуры:
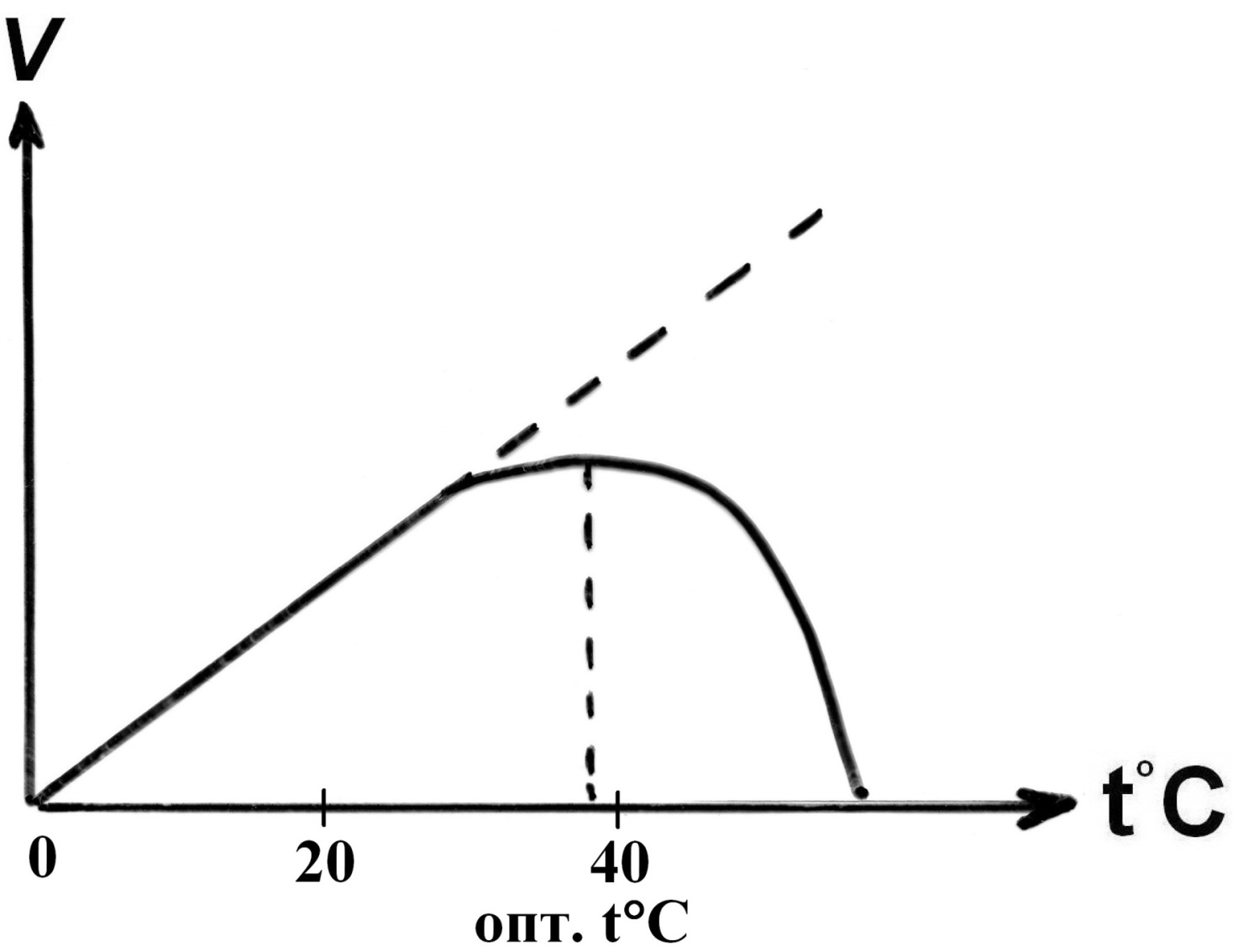
При нагревании:
рвутся слабые связи в молекуле фермента (гидрофобные, ионные и водородные) => меняется конформация E => нарушается структура активного центра E => уменьшается активность E.
III. Зависимость скорости реакции от pH среды:
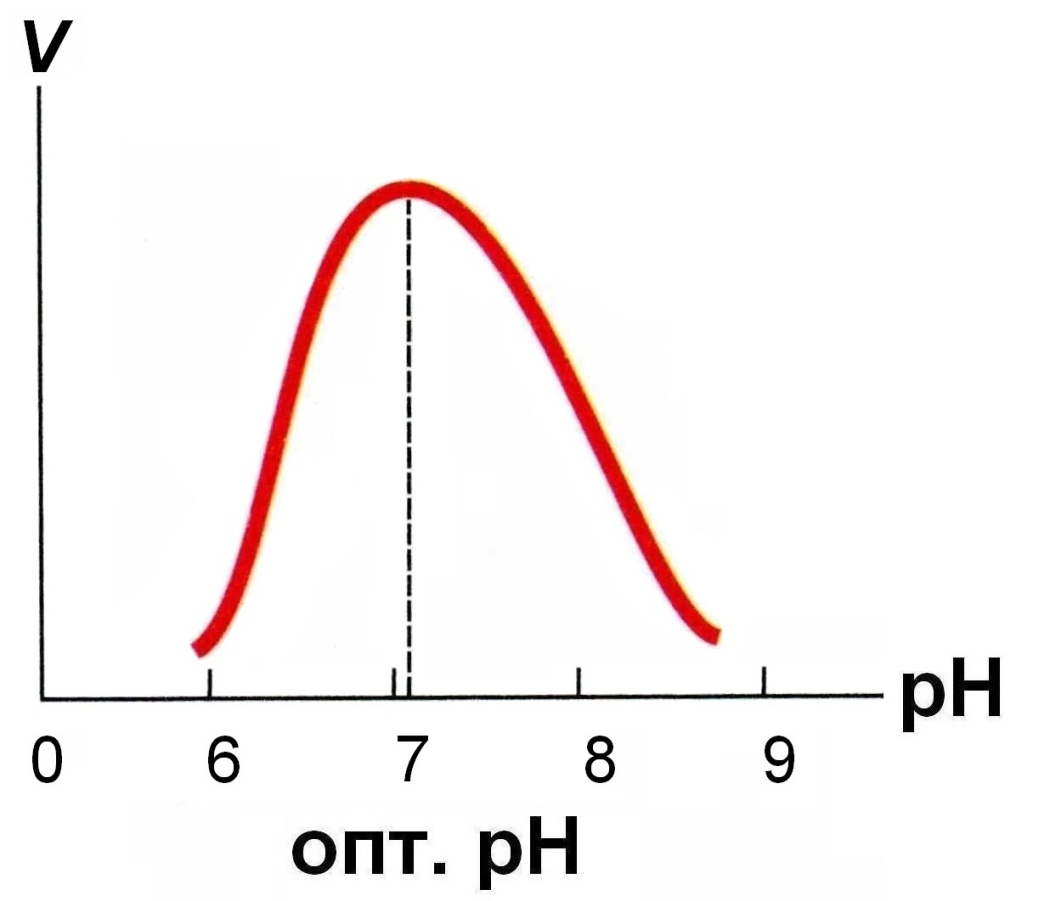
Оптимум pH – это такое значение pH, при котором E проявляет максимальную активность.
Для каждого E характерен довольно узкий интервал pH, при котором он активен:
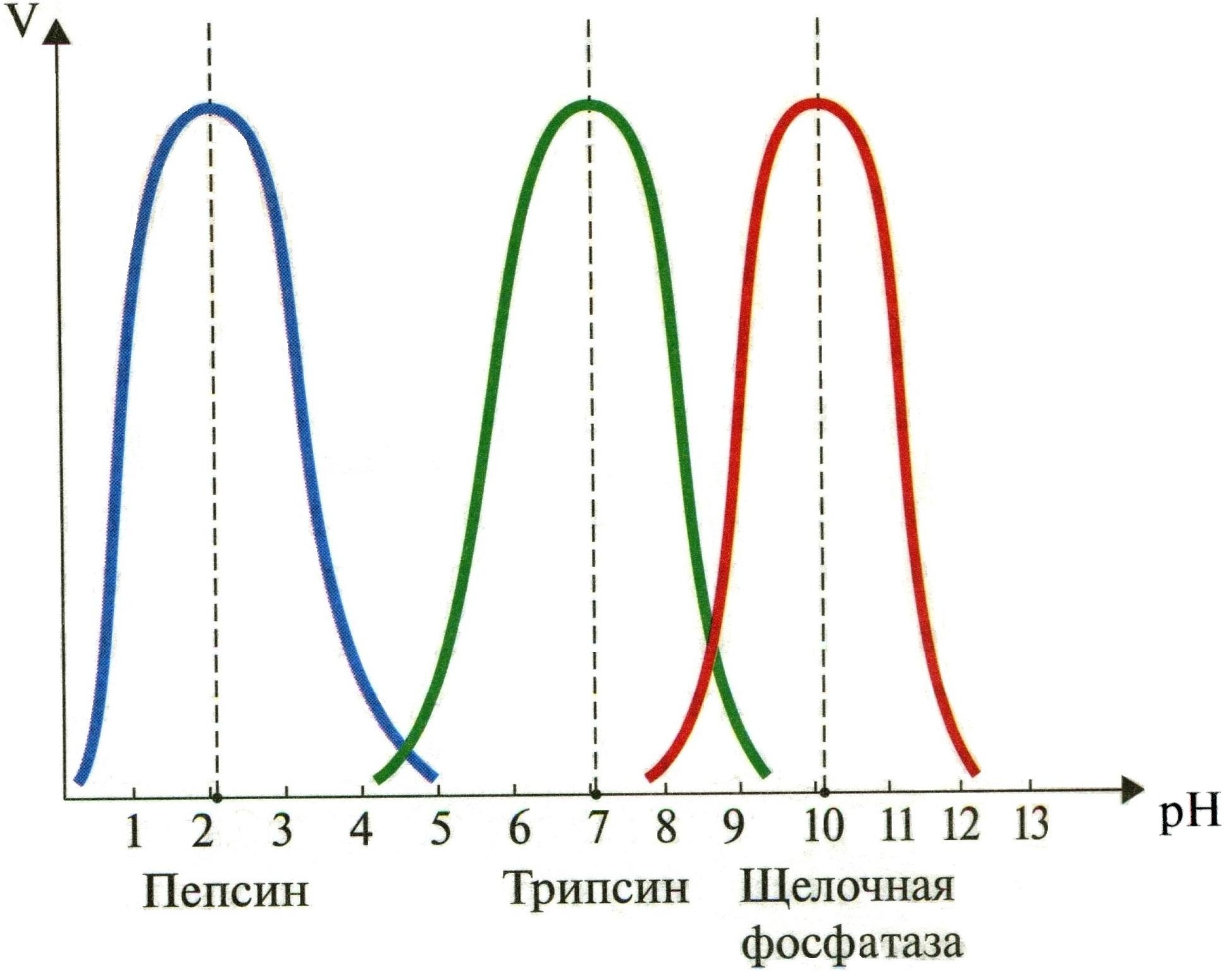
При изменении pH среды в сторону от оптимума активность E уменьшается:
Причины:
изменяется ионизация ионогенных групп => рвутся ионные и некоторые водородные связи в молекуле фермента => меняется конформация E => нарушается структура активного центра E => уменьшается активность E.

Кофакторы ферментов и их роль в катализе.
Если фермент является сложным белком, то в его состав всегда входит небелковый компонент, который называется: Кофактор.
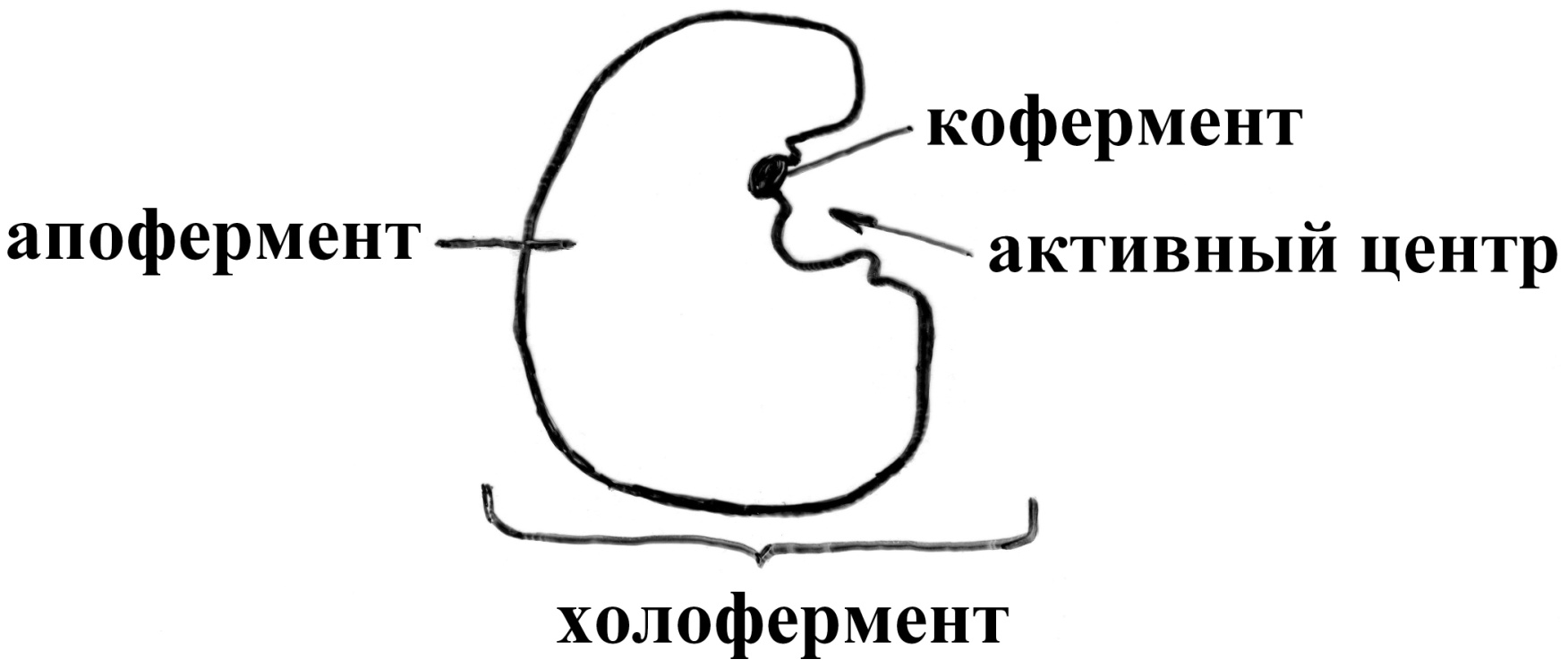
Белковая часть такого фермента называется: Апофермент.
А комплекс апофермента с кофактором получил название: Холофермент:
Апофермент + Кофактор Холофермент
Каталитическую активность в этом случае проявляет только Холофермент.
Кофакторы
Коферменты Ионы металлов
Роль ионов металлов в катализе:
1) участвует в присоединении субстрата (Mg2+, Mn2+, Zn2+)
2) принимают участие в катализе (Zn2+, Cu2+, Fe2+)
3) принимают участие в стабилизации третичной и четвертичной структуры фермента (K+, Ca2+, Zn2+)
4) активаторы ферментов (Ca2+)
Коферменты:
1) органические вещества, предшественниками которых, как правило, являются витамины;
Принимают непосредственное участие в катализе, наряду с радикалами аминокислот.
Некоторые коферменты непрочно связаны с апоферментом (NAD+, NADP+, HS-KoA, H4-фолат).
Есть коферменты, прочно связанные с апоферментом, т.е. представляют с собой простетическую группу (гем, FAD, FMN, биотин).
Примеры коферментов
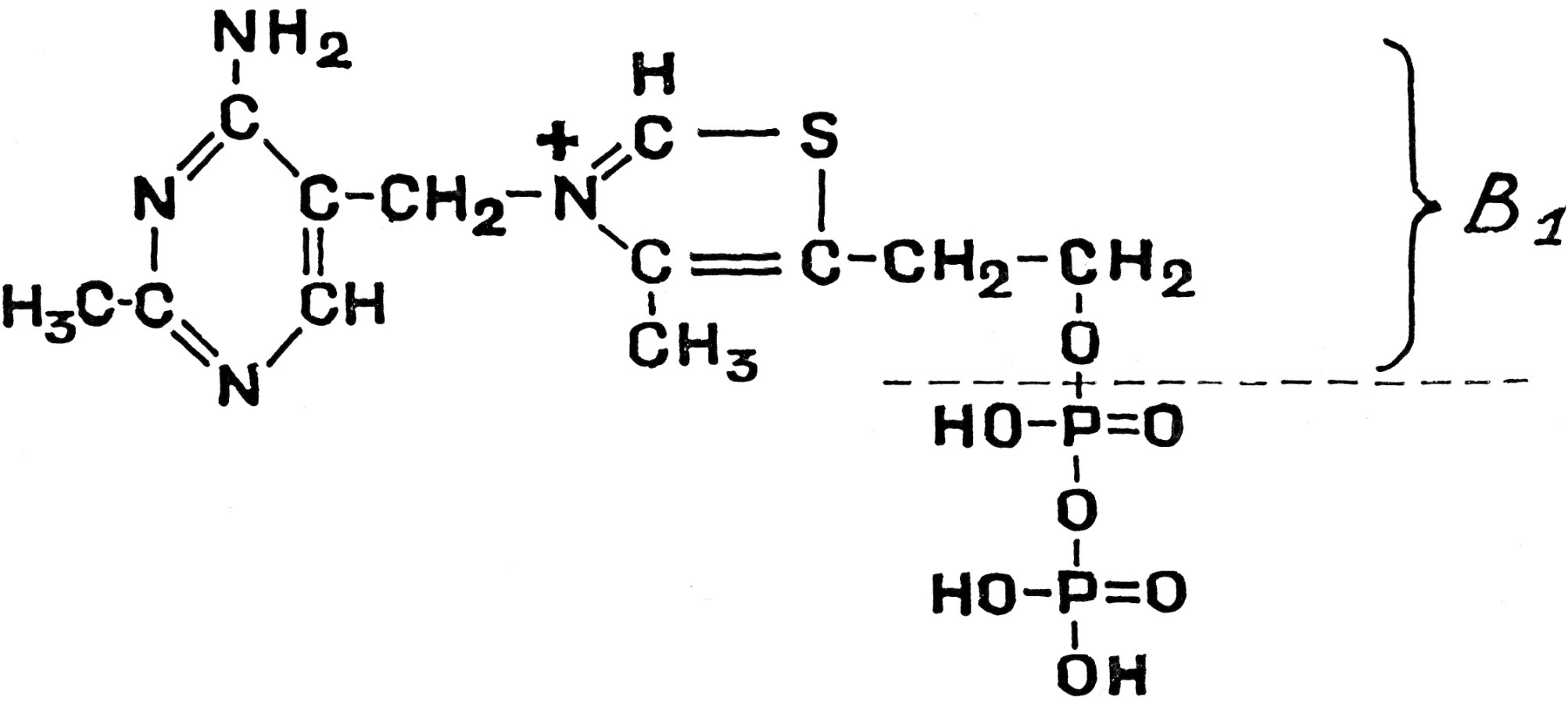
Тиаминдифосфат (ТДФ):
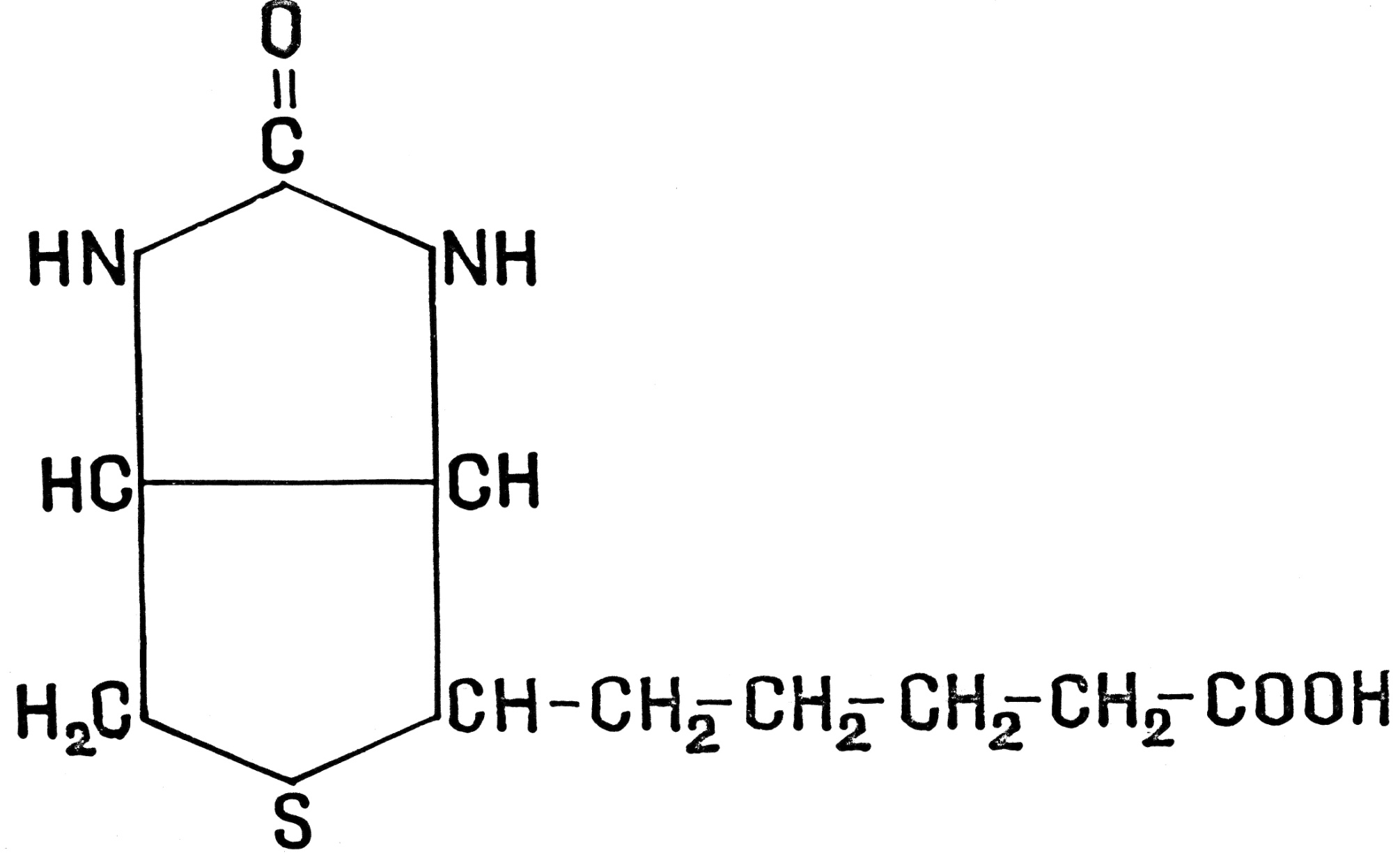
Биотин (витамин H):
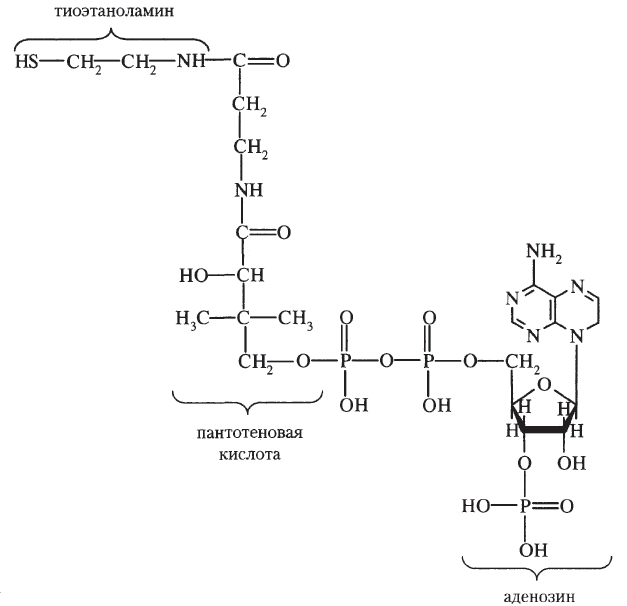
Кофермент A:
Классификация ферментов.
|
из
5.00
|
Обсуждение в статье: IV этап: выход продуктов из области активного центра фермента.) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

