 |
Главная |
Спецглавы физических и химических наук
|
из
5.00
|
Задачи к зачету
(магистратура «Биология», очно-заочное отделение)
Тема: Химическая термодинамика и химическое равновесие
1. При сгорании 21,5 г ацетона выделяется 660,72 кДж. Составьте термохимическое уравнение этой реакции.
2. В калориметрической бомбе в избытке хлора сожгли 0,0123 г алюминия. В результате выделилось 320,8 Дж теплоты. Вычислите энтальпию образования хлорида алюминия.
3. Определите энтальпию реакции COCl2 + ½ O2 = CO2 + Cl2 по следующим данным:
COCl2 = CO + Cl2, ΔHo = 112,5 кДж
CO2 = CO + ½ O2, ΔHo = 282,8 кДж
4. Подберите коэффициенты в уравнениях реакций. Используя табличные данные энтальпий образования участников, рассчитайте тепловые эффекты следующих реакций:
SiCl4(г) + H2O(г) → SiO2(кр) + HCl(г)
H2O(г) + Br2(г) → HBr(г) + O2(г)
NH3(г) + NO2(г) → N2(г) + H2O(г)
Al(кр) + CuO(кр) → Cu(кр) + Al2O3 (кр)
Запишите термохимические уравнения реакций.
5. Одной из стадий количественного определения антиангинального препарата нитроглицерина является реакция:
 .
.
Вычислите тепловой эффект реакции. Какой экзо- или эндотермической она является?
6. Энтальпия сгорания мочевины с образованием углекислого газа и жидкой воды равна –635 кДж/моль. Рассчитайте энтальпию образования мочевины из простых веществ, если известны энтальпии образования углекислого газа и жидкой воды ΔHo f (CO2) = –393,51 кДж/моль, ΔHo f (H2O) = –285,8 кДж/моль.
7. Энтальпии сгорания α-глюкозы, β-фруктозы и сахарозы при 25°С равны соответственно –2802, –2810 и –5644 кДж/моль. Рассчитайте теплоту гидролиза сахарозы.
8. В организме человека в результате метаболизма образуется глицерин, который далее превращается в СО2(г) и Н2О(ж). Пользуясь справочными данными энтальпий образования, определите, какое количество теплоты выделяется при окислении 1 г глицерина.
9. Рассчитайте энтальпию реакции получения мочевины в организме из аммиака и оксида углерода (IV) 2NH3(г) + СО2(г) = СO(NH2)2(т) + Н2О(г).
10. Вычислите стандартные энтропии реакций радикального хлорирования метана до хлорметана и этана до хлорэтана. Какая из реакций характеризуется более существенным приращением стандартной энтропии?
11. Какая из реакций гидрирования: а) пропена; б)1,2–бутадиена будет характеризоваться максимальным значением энтропии.
12. Оцените роль энтальпийного и энтропийного фактора для реакции диспропорционирования нитрита натрия:
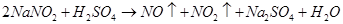 .
.
Возможно ли самопроизвольное протекание этой реакции при стандартных условиях?
13. Оцените роль энтальпийного и энтропийного факторов для реакции ферментативного гидролиза мочевины.

Возможно ли самопроизвольное протекание этой реакции при стандартных условиях?
14. Для реакции гидратации яичного альбумина при 25ºС ΔHo=–6,58 кДж/моль, ΔSo=–9,5 Дж/моль∙К. Найдите константу равновесия для этой реакции.
15. Вычислить константу равновесия и начальные концентрации веществ для реакции  , если равновесные концентрации веществ участников реакции равны: 2, 1, 3,2 моль/л соответственно.
, если равновесные концентрации веществ участников реакции равны: 2, 1, 3,2 моль/л соответственно.
Тема: Коллигативные свойства растворов
1. Найдите температуры замерзания и кипения следующих водных растворов:
а) 5%-ный раствор глюкозы;
б) 10%-ный раствор мочевины:
в) 10%-ный раствор сахара.
Криоскопическая и эбуллиоскопическая константы воды соотвественно равны 1,86 К∙кг/моль и 0,512 К∙кг/моль.
2. При какой температуре закипит 2%-ный спиртовой раствор салициловой кислоты, применяемый как антисептическое средство? Эбулископическая константа этанола 1,11 К×кг/моль. Температура кипения этанола 78ºС.
3. Гормон адреналин состоит (по массе) из 59% углерода, 26,2 % кислорода, 7,1% водорода и 7,6% азота. Температура кипения раствора, содержащего 6,4 г адреналина в 360 г, на 0.49 К выше температуры кипения чистого СCl4. Какова молярная масса и молекулярная формула адреналина (Эбулиоскопическая константа для СCl4 равна 5,02 К×кг/моль)?
4. Для определения молекулярной массы белого фосфора его навеску 0,7590 г растворили в 30 г бензола, температура кристаллизации полученного раствора равна 4,5 0С. Найдите, сколько атомов входит в молекулу белого фосфора. Температура кристаллизации чистого бензола равна 5,50С, К=4,9 К×кг/моль.
5. Определите температуру замерзания раствора хлорида натрия массовой долей 5 %, если кажущаяся степень диссоциации NaCl в этом растворе равна 84,5 %. Криоскопическая постоянная воды 1,86 К×кг/моль.
6. Найдите, при какой температуре закипит и замерзнет 5%-ный раствор перманганата калия, считая степень его диссоциации в этом растворе равной 83%.
7. Вычислите изотонический коэффициент в 0,15 М растворе NaCl, который изотоничен 5%-му раствору глюкозы (плотность раствора глюкозы считать равной 1г/мл).
8. Определите молярную концентрацию раствора сахарозы, который изотоничен крови.
9. Чему равна осмоляльная концентрация крови лягушки, если температура замерзания крови равна –0,41°С?
10. Определить осмотическое давление крови лягушки, если осмотическая концентрация ее крови при 7°С равна 220 мОсмоль/л.
11. Определить процентную концентрацию раствора NaCl, который изотоничен крови лягушки, если осмотическая концентрация ее крови равна 220 мОсмоль/л.
12. Какое явление (лизиса или плазмолиза) эритроцитов при 20°С будет наблюдаться в 30%-ном растворе тиосульфата натрия (ρ=1,274 г/мл), если осмотическое давление крови составляет 730–780 кПа? Степень диссоциации Na2S2O3 считать равной 0,9.
Тема: Протолитические равновесия. рН растворов. Буферные системы
Необходимые для решения задач значения констант диссоциации кислот и оснований приведены в таблице.
1. В таблице приведены значения рН некоторых жидкостей. Найдите концентрацию ионов водорода и гидроксид-ионов.
| Раствор | рН |
| Прохладительные напитки | 2,0 – 4,0 |
| Лимонный сок | 2,2–2,4 |
| Уксус столовый | 2,4–3,4 |
| Томатный сок | 4,0–4,4 |
| Черный кофе | 5,0–5,1 |
| Молоко | 6,3–6,6 |
| Чистая вода | 7,0 |
| Плазма крови | 7,35–7,45 |
| Желчь | 7,6–8,6 |
| Сок поджелудочной железы | 7,8–8,0 |
| Раствор мыла | 8–10 |
2. В нормальном желудочном соке содержание соляной кислоты колеблется в пределах от 0,07 до 0,15%. Рассчитать пределы изменения рН. Плотность желудочного сока принять равной 1 г/мл.
3. К 49 мл воды добавлено 5 мл 0,1 н NaOH. Как изменилось значение рН?
4. К 49 мл воды добавлено 3 мл 0,1 н HCl. Как изменилось значение рН?
5. Три кислоты имеют следующие значения рКа: масляная кислота – 4,82, барбитуровая кислота – 5,0, молочная кислота – 3,85. Какая из них является самой слабой и какая самой сильной? Найдите значения констант ионизации кислот.
6. Найдите значение рН раствора молочной кислоты с концентрацией 0,15 моль/л. Чему равна степень диссоциации молочной кислоты в этом растворе?
7. Вычислите рН раствора, полученного при растворении таблетки аскорбиновой кислоты массой 0,5 г в таком количестве воды, чтобы объем раствора достигал 0,4 л (Ка = 8,0∙10–5 моль/л, молекулярная формула аскорбиновой кислоты С6Н8О6).
8. Найдите значение рН нашатырного спирта (10%-ного водного раствора аммиака). Плотность раствора принять равной 0,96 г/мл.
9. Найдите значения рН буферных смесей, содержащих эквимолярные количества (а) Н3ВО3 и Н2ВО3– ;(б) НСО3– и СО32–; (в) H3PO4 и H2PO4–.
10. Рассчитайте рН буферного раствора, полученного растворением 0,1 моль муравьиной кислоты и 0,1 моль формиата натрия в 1 литре воды. Рассчитайте массы реагентов для получения такого раствора.
11. рН раствора, полученного растворением 1 моль пропионовой кислоты и 1 моль пропионата натрия в 1 л воды, составляет 4,85. Каково будет значение рН при использовании по 0,1 моль каждого из реагентов?
12. Рассчитайте рН водных растворов, содержащих:
а) 0,58 моль/л уксусной кислоты и 0,18 моль/л ацетата натрия;
б) 0,8 моль/л молочной кислоты и 0,4 моль/л лактат-иона;
в) 0,42 моль/л фтороводородной кислоты и 1,38 моль/л фторида натрия;
г) 0,3 моль/л NH4OH и 1,48 моль/л NH4+.
13. Сколько граммов твердого Na2HPO4 необходимо добавить к 1 л 0,01 M раствора NaH2PO4, чтобы получить раствор с рН равным 8,21?
14. Каково соотношение концентраций H2CO3 и гидрокарбонат-анионов, а также анионов H2PO4– и HPO42– в плазме крови при физиологически нормальном значении рН?
Константы диссоциации некоторых кислот и оснований в водных растворах при 25 ºС
| Ka | pKa | ||
| HF | 6,67∙10–4 | 3,16 | |
| H2CO3 | K1 K2 | 4,27∙10–7 4,68∙10–11 | 6,37 |
| H3BO3 | K1 K2 K3 | 5,75∙10–10 1,8∙10–13 1,6∙10–14 | 9,24 12,74 13,80 |
| CH3COOH | 1,75∙10–5 | 4,75 | |
| HCOOH | 1,78∙10–4 | 3,75 | |
| Молочная кислота CH3CH(OH)COOH | 1,48∙10–4 | 3,83 | |
| H3PO4 | K1 K2 K3 | 7,2∙10–3 6,2∙10–8 4,6∙10–13 | 2,14 7,21 12,35 |
| Kb | pKb | ||
| NH4OH | 1,75∙10–5 | 4,75 |
|
из
5.00
|
Обсуждение в статье: Спецглавы физических и химических наук |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

