 |
Главная |
Задачи для самостоятельного решения. 5.1. Написать в ионно-молекулярной форме уравнения реакций
|
из
5.00
|
5.1. Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малорастворимых осадков или газов:
а) Pb(NO3)2 + KI; б) NiCl2 + H2S; в) K2CO3 + HCl; г) CuSO4 + NaOH;
д) CaCO3 + HCl; е) Na2SO3 + H2SO4; ж) AlBr3 + AgNO3.
5.2. Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малодиссоциированных соединений: а) Na2S + H2SO4; б) FeS + HCl; в) HCOOK + HNO3; г) NH4Cl + Ca(OH)2; д) NaOCl + HNO3.
5.3. Написать в ионно-молекулярной форме уравнения реакций нейтрализации: а) HCl + Ba(OH)2; б) HF + KOH; в) Fe(OH)3 + HNO3; г) CH3COOH + NH4OH; д) HNO2 + NH4OH; е) H2S + NH4OH.
Указать, какие из этих реакций протекают обратимо, а какие – необратимо.
5.4. Составить в молекулярной форме уравнения реакций, которые выражаются следующими ионно-молекулярными уравнениями:
NO2– + H+ = HNO2;
Cu2+ + 2OH– = Cu(OH)2↓;
Pb2+ + 2I – = PbI2↓.
5.5. Написать в ионно-молекулярной форме уравнения реакций взаимодействия между водными растворами следующих веществ: а) NaHСO3 и HCl; б) FeCl3 и KOH; в) Pb(CH3COO)2 и Na2S; г) KHS и H2SO4; д) Zn(NO3)2 и KOH (избыток); е) Ca(OH)2 и CO2; ж) Ca(OH)2 и CO2 (избыток).
Для каждого случая указать причину смещения равновесия в сторону прямой реакции.
5.6. В каком направлении будет смещено равновесие реакции
AgI (к.) + NaCl (водн.)  AgCl (к.) + NaI (водн.):
AgCl (к.) + NaI (водн.):
а) в направлении прямой реакции; б) в направлении обратной реакции?
5.7. В каком направлении будет смещено в водном растворе равновесие реакции
CH3COONa+CH2ClCOOH  CH3COOH+CH2ClCOONa:
CH3COOH+CH2ClCOONa:
а) в направлении прямой реакции; б) в направлении обратной реакции?
ВАРИАНТЫ ДОМАШНИХ ЗАДАНИЙ
| Вариант | Номера задач | |||||||
| 1.9 | 1.2(а) | 3.6 | 2.1 | 2.16 | 4.2(а,в) | 4.19 | 5.6 | |
| 1.1 | 1.3 | 3.1 | 2.2 | 2.17 | 4.3(а,б) | 4.7 | 5.1(в,г) | |
| 1.4 | 1.7 | 3.2 | 2.3 | 2.18 | 4.3(б,в) | 4.17 | 5.5(а,ж) | |
| 1.6 | 1.1 | 3.3 | 2.4 | 2.19 | 4.1(а,б) | 4.11 | 5.4 | |
| 1.8 | 1.2(б) | 3.4 | 2.5 | 2.20 | 4.5 | 4.18 | 5.3(а,б) | |
| 1.9 | 1.3 | 3.5 | 2.6 | 2.25 | 4.6 | 4.9(а,г) | 5.3(в,г) | |
| 1.7 | 1.4 | 3.15 | 2.7 | 2.17 | 4.1(а,в) | 4.12 | 5.3(д,е) | |
| 1.5 | 1.10 | 3.7 | 2.8 | 2.20 | 4.8 | 4.16(а,в) | 5.5(е,ж) | |
| 1.1 | 1.8 | 3.8 | 2.9 | 2.24 | 4.2(а,б) | 4.22 | 5.7 | |
| 1.10 | 1.2(в) | 3.9 | 2.10 | 2.14 | 4.13 | 4.16(б,в) | 5.5(д,е) | |
| 1.11 | 1.4 | 3.10 | 2.1 | 2.26 | 4.4(а,б) | 4.15 | 5.2(г,д) | |
| 1.2(г) | 1.7 | 3.11 | 2.12 | 2.27 | 4.10 | 4.18 | 5.5(г,д) | |
| 1.3 | 1.9 | 3.14 | 2.13 | 2.10 | 4.4(б,в) | 4.20 | 5.1(а,б) | |
| 1.1 | 1.11 | 3.12 | 2.14 | 2.30 | 4.14 | 4.21 | 5.5(б,в) | |
| 1.5 | 1.10 | 3.13 | 2.15 | 2.29 | 4.9(б,в) | 4.13 | 5.1(е,ж) |
ПРИЛОЖЕНИЕ
Таблица 1
Константы диссоциации некоторых слабых
электролитов в водных растворах при 25оС
| Электролит | Константа диссоциации | ||
| Азотистая кислота | HNO2 | 2,6∙10-5 | |
| Аммония гидроксид | NH4OH | 4∙10-4 | |
| Борная кислота | H3BO3 | 5,8∙10-4 | |
| Бромноватистая кислота | HOBr | 2,1∙10-9 | |
| Водорода пероксид | H2O2 | 2,6∙10-12 | |
| Кремниевая кислота | H2SiO3 | K1 K2 | 2,2∙10-10 1,6∙10-12 |
| Муравьиная кислота | HCOOH | 1,8∙10-4 | |
| Сернистая кислота | H2SO3 | K1 K2 | 1,6∙10-2 6,3∙10-8 |
| Сероводород | H2S | K1 K2 | 6∙10-8 1∙10-14 |
| Угольная кислота | H2CO3 | K1 K2 | 4,5∙10-7 4,7∙1011 |
| Уксусная кислота | CH3COOH | 1,8∙10-5 | |
| Фосфорная кислота | H3PO4 | K1 K2 K3 | 7,5∙10-3 6,3∙10-8 1,3∙10-12 |
| Циановодород | HCN | 7,9∙10-10 | |
| Щавелевая кислота | H2C2O4 | K1 K2 | 5,4∙10-2 5,4∙10-5 |
Таблица 2
Произведение растворимости некоторых
малорастворимых электролитов при 25оС
| Электролит | ПР | Электролит | ПР | Электролит | ПР |
| AgBr | 5,3·10-13 | CaSO4 | 6,1·10-5 | MnS | 2,5·10-10 |
| Ag2CO3 | 8,2·10-12 | Ca3(PO4)2 | 1,0·10-29 | Ni(OH)2 | 6,3·10-18 |
| AgCl | 1,8·10-10 | CdS | 1,6·10-28 | PbBr2 | 9,1·10-6 |
| Ag2CrO4 | 1,1·10-12 | CoCO3 | 1,5·10-10 | PbCO3 | 7,5·10-14 |
| AgI | 8,3·10-17 | Co(OH)2 | 2·10-16 | PbCl2 | 1,56·10-5 |
| Ag2S | 5,3·10-50 | CrPO4 | 2,4·10-23 | PbF2 | 2,7·10-8 |
| Ag2SO4 | 1,6·10-5 | CuCO3 | 2,5·10-10 | PbI2 | 1,1·10-9 |
| Ag3PO4 | 1,3·10-20 | Cu(OH)2 | 1,6·10-19 | PbS | 2,5·10-27 |
| Al(OH)3 | 5·10-33 | CuS | 6,3·10-36 | PbSO4 | 1,6·10-8 |
| AlPO4 | 5,7·10-19 | Fe(OH)2 | 8·10-16 | Pb3(PO4)2 | 7,9·10-43 |
| BaCO3 | 5,1·10-9 | Fe(OH)3 | 6,3·10-38 | Sb2S3 | 1,6·10-93 |
| BaCrO4 | 1,2·10-10 | FePO4 | 1,3·10-22 | SrCO3 | 1,1·10-10 |
| BaSO4 | 11·10-10 | FeS | 5·10-18 | SrCrO4 | 3,6·10-5 |
| Ba3(PO4)2 | 6,0·10-39 | HgS | 1,6·10-52 | SrF2 | 2,5·10-9 |
| BeCO3 | 1·10-3 | MgCO3 | 2,1·10-5 | SrSO4 | 3,2·10-7 |
| CaCO3 | 4,8·10-9 | Mg(OH)2 | 6·10-10 | ZnCO3 | 1,4·10-14 |
| CaF2 | 4,0·10-11 | Mg3(PO4)2 | 1·10-13 | Zn(OH)2 | 1·10-17 |
| CaHPO4 | 2,7·10-7 | MnCO3 | 1,8·10-11 | α-ZnS | 1,6·10-24 |
| Ca(H2PO4)2 | 1·10-3 | Mn(OH)2 | 1,9·10-13 | Zn3(PO4)2 | 9,1·10-33 |
Таблица 3
| Ионная сила раствора I | Заряд иона z | Ионная сила раствора I | Заряд иона z | |||||
| ±1 | ±2 | ±3 | ±1 | ±2 | ±3 | |||
| 0,001 | 0,98 | 0,78 | 0,73 | 0,1 | 0,81 | 0,44 | 0,16 | |
| 0,002 | 0,97 | 0,74 | 0,66 | 0,2 | 0,80 | 0,41 | 0,14 | |
| 0,005 | 0,95 | 0,66 | 0,55 | 0,3 | 0,81 | 0,42 | 0,14 | |
| 0,01 | 0,92 | 0,60 | 0,47 | 0,4 | 0,82 | 0,45 | 0,17 | |
| 0,02 | 0,90 | 0,53 | 0,37 | 0,5 | 0,84 | 0,50 | 0,21 | |
| 0,05 | 0,84 | 0,50 | 0,21 |
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
1. Ахметов Н.С. Общая и неорганическая химия. - М.: Высшая школа, 2002.-743 с.
2. Глинка Н.Л., Ермаков А.И. Общая химия. - М.: Интеграл-пресс, 2004 - 728 с.
3. Карапетъянц М.Х., Дракин С.И. Общая и неорганическая химия. - М.: Химия, 2000 – 532 с..
4. Глинка Н.Л. Задачи и упражнения по общей химии. 2004, М. «Интеграл-Пресс», с. 240.
Задание №6
По теме: «ГИДРОЛИЗ СОЛЕЙ»
Вопросы и задачи для самостоятельного решения
1. Написать ионно-молекулярные уравнения реакции гидролиза с указанием pH при растворении в воде следующих солей: сульфата цинка, нитрата калия, хлорида цезия, сульфата хрома (III).
2. Написать в ионно-молекулярной форме уравнения гидролиза следующих солей: K2S, K2CO3, Li2S, K3PO4, K2SO3.
3. Написать в молекулярной форме уравнение гидролиза гидросолей и определить pH среды их водных растворов: NaHSO3, NaHS, KHCO3, Na2HPO4, NaH2PO4.
4. Написать в молекулярно-ионной форме уравнение гидролиза солей и указать реакцию их водных растворов: ZnCI2, Cu(NO3)2, FeSO4, AICI3, CrCI3.
5. Написать молекулярно-ионные формы уравнений гидролиза (отдельно для катиона и аниона) и указать реакцию водных растворов солей: (NH4)2S, (NH4)2SO3, (NH4)3PO4, (NH4)2HPO4.
6. Написать молекулярно-ионные формы уравнений гидролиза и указать реакцию водных растворов солей:
а) NH4HS; б) NH4HSO3; в)NH4H2PO4.
7. Написать молекулярно-ионные формы уравнений гидролиза и указать реакцию водных растворов солей:
а) AI(CH3COO)3; б) Fe(HCOO)3; в) Cu(CH3COO)2.
8. Написать в молекулярной и молекулярно-ионной форме уравнения реакций и объяснить механизм их протекания:
 а) Fe2(SO4)3 + Na2CO3 + H2O ......
а) Fe2(SO4)3 + Na2CO3 + H2O ......
б  ) AICI3 + (NH4)2S + H2O ......
) AICI3 + (NH4)2S + H2O ......
 в) Cr2(SO4)3 + (NH4)2S + H2O ......
в) Cr2(SO4)3 + (NH4)2S + H2O ......
9. Написать в молекулярной и молекулярно-ионной форме уравнения реакций и объяснить механизм их протекания:
 а) AICI3 + CH3COONa + H2O AI(OH) (CH3COO)2 + ......
а) AICI3 + CH3COONa + H2O AI(OH) (CH3COO)2 + ......
 б) CuSO4 + Na2CO3 + H2O [Cu(OH)]2CO3 + ......
б) CuSO4 + Na2CO3 + H2O [Cu(OH)]2CO3 + ......
 в) Na2SiO3 + NH4CI + H2O ......
в) Na2SiO3 + NH4CI + H2O ......
10. Указать, не производя вычислений, в каком из растворов двух солей равной концентрации pH больше или меньше (см. табл. ):
а) NaCIO4 и NaCIO ;
б) K2S и K2Se ;
в) Na2CO3 и NaHCO3 .
11. Указать, не производя вычислений, в каком из растворов двух солей равной концентрации pH больше или меньше (см. табл. ).
а) CH3COONa и HCOONa ;
б) Na2CO3 и NaSO3 ;
в) HCOONa и HCOONH4 .
12. Охарактеризовать поведение в растворе следующих солей и указать реакцию их водных растворов: HCOOK, NH4Br, K2HPO4, Cu(NO3)2.
13. Раствор NaH2PO4 имеет слабо кислую, а раствор Na3PO4 имеет сильнощёлочную реакцию. Объяснить эти факты, подтвердить уравнениями.
14. При сливании водных растворов Cr(NO3)3 и Na2S образуется осадок Cr(OH)3 и выделяется газ. Составить молекулярное и ионно-молекулярное уравнение реакций.
15. Какие из перечисленных солей подвергаются гидролизу:
а) NaHCO3; б) NaCN; в) KNO3.
Написать молекулярные и ионно-молекулярные уравнения гидролиза.
16. Вычислить константу гидролиза фторида калия, определить степень гидролиза этой соли в 0,01 М растворе и pH раствора.
17. Вычислить pH 0,02 н. раствора соды Na2CO3, учитывая только первую ступень гидролиза.
18. Сравнить степень гидролиза соли и pH среды в 0,1 М и 0,001 М растворах цинанида калия.
19. При 600С ионное произведение воды КH2O = 10-12. Считая, что константа диссоциации хлорноватистой кислоты не изменяется с температурой, определить pH 0,001Н раствора KOCI при 25 и 600С.
20. pH 0,1М раствора натриевой соли органической одноосновной кислоты равен 10.
Вычислить К диссоциации этой кислоты.
21. Исходя из значений К диссоциации соответствующих кислот и оснований, указать реакцию водных растворов следующих солей: NH4CN, NH4F, (NH4)2S.
22. Почему раствор NaHCO3 имеет слабощелочную среду, а NaHSO3 слабокислую реакцию? Ответ обосновать.
23. Вычислить константу гидролиза карбоната натрия, степень гидролиза соли в 0,1 М растворе и pH среды.
24. Вычислить константу гидролиза ортофосфата калия. Каков pH в 2,4 М растворе Na3PO4? Определить степень гидролиза.
25. Вычислить константу гидролиза ортофосфата калия. Каков pH в 3н. растворе Na3PO4. Какова степень гидролиза?
26. Вычислить константу гидролиза сульфита натрия, степень гидролиза и pH 0,6 М раствора.
27. Вычислите pH 0,2 М раствора NaHCOO, если KHCOOH =1,7∙10-4.
28. Оцените pH раствора, полученного растворением 0,001г NH4CI в 10л воды. KNH4OH = 1,8∙10-5.
29. В чем состоит отличие реакций гидролиза AI(CH3COO)3 и AI2S3 ?
30. Объясните, почему при введении в раствор FeCI3 раствора соды в осадок выпадает не карбонат железа, а его гидроксид. Напишите уравнение процессов.
31. Составьте уравнение реакций, протекающих в водных растворах:
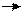 а) AICI3 + H2O
а) AICI3 + H2O
 б) AICI3 + (NH4)2S + H2O
б) AICI3 + (NH4)2S + H2O
 в) AICI3 + (NH4)2CO3 + H2O
в) AICI3 + (NH4)2CO3 + H2O
32. Предполагают, что гидролиз буры протекает в 2 стадии:
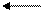
 B4O72- + 3H2O 2H3BO3 + 2BO2-
B4O72- + 3H2O 2H3BO3 + 2BO2-

 BO2- + 2H2O H3BO3 + OH-
BO2- + 2H2O H3BO3 + OH-
Как рассчитать pH раствора буры известной концентрации ?
33. Вычислите pH раствора, в 5л которого содержится 20 г NH4CI, если KNH4OH = 1,8∙ 10-5.
34. У какого раствора pH больше: SnCI2 или SnCI4 (при одинаковых концентрациях)?
35. Отличается ли гидролиз AICI3 от AIF3? Ответ обосновать уравнениями.
36. Приведите возможные способы смещения равновесия реакций гидролиза вправо и влево.
37. Приготовлены растворы солей Na2CO3, FeCI3 и CuSO4. Напишите по-стадийно уравнения гидролиза. Как осуществить последнюю стадию гидролиза ?
38. Расположите соединения Na2CO3, NaHCO3 и NaOH в порядке увеличения pH их растворов одинаковой концентрации.
39. Напишите сокращенным молекулярно-ионным способом уравнения реакций гидролиза следующих солей:
1) FeCI3; 2) Fe2(SO4)3; 3) Fe(OH)CI2.
40. Напишите сокращённое молекулярно-ионное уравнение реакций гидролиза следующих солей:
1) NaNO3; 2) NH4NO2; 3) NH4NO3.
41. Напишите сокращённое молекулярно-ионное уравнение реакций гидролиза следующих солей:
1) Zn(NO3)2; 2) Cu(NO3)2; 3)Ca(NO2)2.
42. Напишите сокращённое молекулярно-ионное уравнение реакций гидролиза следующих солей:
1) Cu(CH3COO)2; 2) CuSO4; 3) Cu(OH)NO3.
Укажите реакцию среды.
43. Укажите способы смещения равновесия реакций гидролиза вправо:

 CO32- + H2O HCO3- + OH-
CO32- + H2O HCO3- + OH-

 HCO3- + H2O H2CO3 + OH-
HCO3- + H2O H2CO3 + OH-
44. Какие соли железа гидролизуются сильнее: FeCI2 или FeCI3 и почему? Ответ обосновать.
45. Вычислите pH 0,1 М раствора NH4CI (KNH4OH = 1,8 ∙10-5).
46. Раствор, содержащий в 1л 3,81 г тетрабората натрия Na2B4O7 ∙ 10H2O (бура), имеет pH = 9,18. Напишите уравнение реакции гидролиза и вычислите константу первой стадии гидролиза, предполагая, что она обусловливает щёлочную среду раствора.
47. Вычислите константу диссоциации BeOH+
BeOH+ = Be2+ + OH-
исходя из того, что pH 2 ∙ 10-2М раствора BeCI2 составляет 4,2.
48. Соли, образованные многоосновными кислотами и многокислотными основаниями, гидролизуются по ступеням. Докажите, что полная константа гидролиза равна произведению константы гидролиза всех ступеней гидролиза.
49. Вычислите pH 0,2 М раствора NaHCOO, если KНСООН = 1,8 ∙ 10-4.
50.Напишите сокращенное молекулярно-ионное уравнение реакций гидролиза следующих солей (если возможно):
NaCIO4, NH4CIO4, Na2S.
51. При каких условиях можно ожидать (теоретически) нейтральную реакцию среды раствора соли ?
52. Реакция среды водного раствора MgCI2 нейтральна. О чём это говорит?
53. Напишите сокращенное молекулярно-ионное уравнение реакций гидролиза следующих солей:
NaCH3COO, NH4CH3COO, Fe(OH)SO4.
54. Водные растворы HCI и FeCI3 показывают кислую среду. Это объясняется протеканием следующих процессов:
HCI + H2O = H2O+ +CI-
FeCI3 + 2H2O H3O+ + CI- + FeOHCI2
Укажите признаки сходства и различия этих процессов. Назовите процессы.
55. Разбавленные растворы LiJ и CsF нейтральны. По мере повышения концентрации раствор LiJ начинает показывать кислую реакцию, а раствор CsF - щёлочную. Как это объяснить ?
56. Предскажите реакцию среды (кислая или щёлочная) водных растворов Na3PO4, Na2HPO4 и NaH2PO4.
57. Напишите сокращенное молекулярно-ионное уравнение реакций гидролиза следующих солей:
Fе(NO3)3, Fe(OH)2NO3, Cu(NO3)2.
58. Определите pH 0,1 М раствора ортофосфата калия.
59. У какого раствора рН больше: FeCl2 или FeCl3 (при одинаковых концентрациях)?
60. Определите рН 0,1 М раствора дегидрофосфата калия.
Варианты контрольных заданий
| Вариант | Номер задачи | |||
Примеры решения задач
Пример 1. Вычислить степень гидролиза цианида калия при концентрации 0,1 и 0,001 г-экв/л, если константа диссоциации HCN=7,2∙10-10.
Решение:
1) Запишем уравнение диссоциации HCN:
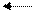
 HCN H+ + CN-
HCN H+ + CN-
KHCN = 
2) Запишем уравнение гидролиза KCN в 3-х формах:
а) молекулярной

 KCN + H2O HCN + KOH;
KCN + H2O HCN + KOH;
 б) ионно-молекулярной
б) ионно-молекулярной


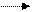 K+ + CN- + H2O HCN + K+ + OH- ;
K+ + CN- + H2O HCN + K+ + OH- ;
в) в краткой ионно-молекулярной форме

 CN- + H2O HCN + OH- .
CN- + H2O HCN + OH- .
Подставляем данные значения в формулу определения степени гидролиза:
h = 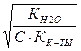 =
=  = 0.0118,
= 0.0118,
% = 0.011∙8100 = 1.18%; h = 1,18 .
Для с= 0,001  имеем h =
имеем h = 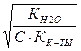 =
=  = 0.118 или
= 0.118 или
1,18%.
Пример 2. Вычислить К гидролиза, h и pH 0,1 моль/л раствора CH3COONa.
Решение:
Запишем уравнение гидролиза CH3COONа в 3-х формах:
а) молекулярной
 CH3COONa + H2O CH3COOH + NaOH;
CH3COONa + H2O CH3COOH + NaOH;
б) ионно-молекулярной

 CH3COO- + Na+ + H2O CH3COOH + Na+ + OH- ;
CH3COO- + Na+ + H2O CH3COOH + Na+ + OH- ;
в) краткой ионно-молекулярной

 CH3COO- + H2O CH3COOH + OH- .
CH3COO- + H2O CH3COOH + OH- .
Kг =  ,
,
KCH3COOH = 1,74 ∙10-5 ,
KH2O = 10-14 ,
Kг = 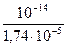 = 5,7 ∙10-10 ;
= 5,7 ∙10-10 ;
степень гидролиза h определяем по формуле
h = 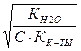 =
= 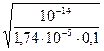 = 7,4∙10-5 или h = 0,0076 %
= 7,4∙10-5 или h = 0,0076 %
[OH-]- = c ∙ h
[OH-] = 10-1 ∙ 7,6 ∙ 10-6 моль;
ионное произведение воды
[H+] ∙ [OH-] = KH2O ,
отсюда [H+] =  ; pH = - Ig [H+],
; pH = - Ig [H+],
pH = - Ig  ≈ 6,88 .
≈ 6,88 .
Пример 3. Вычислить, чему равна константа гидролиза, h и pH 0,1 моль/л раствора фосфата натрия Na3PO4.
Решение:
Запишем уравнение гидролиза по 3-м ступеням в 3-х формах:
I ступень:
а) молекулярная

 Na3PO4 + H2O Na2HPO4 + NaOH;
Na3PO4 + H2O Na2HPO4 + NaOH;
б) ионно-молекулярная




 3Na+ + PO43- + H2O 2Na+ + (HPO4)2- + Na+ + OH- ;
3Na+ + PO43- + H2O 2Na+ + (HPO4)2- + Na+ + OH- ;
в) краткая ионно-молекулярная

 PO43- + H2O HPO42- + OH- .
PO43- + H2O HPO42- + OH- .
II ступень:
а) молекулярная

 Na2HPO4 + H2O NaH2PO4 + NaOH;
Na2HPO4 + H2O NaH2PO4 + NaOH;
б) ионно-молекулярная




 2 Na+ + HPO42- + H2O Na+ + H2PO-4 + Na+ + OH- ;
2 Na+ + HPO42- + H2O Na+ + H2PO-4 + Na+ + OH- ;
в) краткая ионно-молекулярная

 HPO42- + H2O H2PO4- + OH- .
HPO42- + H2O H2PO4- + OH- .
III ступень:
а) молекулярная

 NaH2PO4 + H2O H3PO4 + Na+ + OH- ;
NaH2PO4 + H2O H3PO4 + Na+ + OH- ;
б) ионно-молекулярная

 Na+ + H2PO4- + H2O H3PO4 + NaOH;
Na+ + H2PO4- + H2O H3PO4 + NaOH;
в) краткая ионно-молекулярная

 H2PO4 + H2O H3PO4 + OH- .
H2PO4 + H2O H3PO4 + OH- .
Хотя ионы HPO42- и H2PO4- способны гидролизоваться, однако степени гидролиза ионов HPO42- и H2PO4- малы.
Второй и третьей стадией гидролиза можно пренебречь.
Тогда К гидролиза, h и pH раствора определяем для уравнения

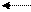 PO43- + H2O HPO4 + OH-
PO43- + H2O HPO4 + OH-
Из табл. 2 имеем:
KH3PO4 = 7,6 ∙ 10-3,
KH2PO4- = 6,2 ∙ 10-8,
KHPO42- = 44 ∙ 10-13,
Кг =  =
=  =
= 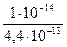 = 0,023.
= 0,023.
Для определения h воспользуемся формулой
h =  =
= 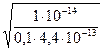 = 0.377, или в процентах 37,7%.
= 0.377, или в процентах 37,7%.
Отсюда
[OH-] = ch = 0,1∙ 0,377 = 3,77 ∙ 10-2,
pOH ≈ 1,42 ,
pH = 10 – 1,42 = 12,6 .
Пример 4. Как будет изменяться pH при растворении в воде солей
1. CuCl2, 2. Na2SO3, 3. K2SO4 ?
Решение:
1) Гидролиз соли CuCI2 проходит ступенчато (в основном по I ступени) по катиону Cu2+.
Первая ступень гидролиза в 3-х формах:
а) молекулярная
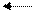
 CuCI2 + H2O Cu(OH)CI + HCI;
CuCI2 + H2O Cu(OH)CI + HCI;
б) ионно-молекулярная


 Cu2+ + 2CI- + H2O (CuOH)+ + CI- + H+ + CI- ;
Cu2+ + 2CI- + H2O (CuOH)+ + CI- + H+ + CI- ;
в) краткая ионно-молекулярная
 Cu2+ + H2O (CuOH)+ + H+ .
Cu2+ + H2O (CuOH)+ + H+ .
Вторая ступень гидролиза практически не протекает:
а) молекулярная

 Cu(OH)CI + H2O (CuOH)2↓ + HCI;
Cu(OH)CI + H2O (CuOH)2↓ + HCI;
б) ионно-молекулярная



 (CuOH)+ + CI- + H2O (CuOH)2↓ + H+ + CI- ;
(CuOH)+ + CI- + H2O (CuOH)2↓ + H+ + CI- ;
в) краткая ионно-молекулярная

 (CuOH)+ + H2O (CuOH)2↓ + H+ .
(CuOH)+ + H2O (CuOH)2↓ + H+ .
2) Гидролиз соли Na2SO3 гидролиз протекает по аниону.
I ступень гидролиза:
а) молекулярная

 Na2SO3 + H2O NaHSO3 + NaOH;
Na2SO3 + H2O NaHSO3 + NaOH;
б) ионно-молекулярная

 2Na+ + SO32- + H2O Na+ + HSO3- + Na+ + OH- ;
2Na+ + SO32- + H2O Na+ + HSO3- + Na+ + OH- ;
в) краткая ионно-молекулярная
 SO32- + H2O HSO3- + OH- .
SO32- + H2O HSO3- + OH- .
II ступень гидролиза:
а) молекулярная
 NaHSO3 + H2O H2SO3 + NaOH ;
NaHSO3 + H2O H2SO3 + NaOH ;
б) ионно-молекулярная

 Na+ + HSO3-+ H2O H2SO3 + Na+ + OH- ;
Na+ + HSO3-+ H2O H2SO3 + Na+ + OH- ;
в) краткая ионно-молекулярная

 HSO3-+ H2O H2SO3 + OH- .
HSO3-+ H2O H2SO3 + OH- .
3) Соль K2SO4 образована сильным основанием (КОН) и сильной кислотой (Na2SO4).
Гидролизу не подвергается, pH = 7.
Пример 5. Закончить уравнение реакции с учётом возможности необратимого гидролиза образуемых солей.
 AI2(SO4)3 + Na2S + H2O ?
AI2(SO4)3 + Na2S + H2O ?
Решение:
Гидролиз в данном случае идёт до конца, так как образуются осадок AI(OH)3 и газ H2S.
Уравнение гидролиза будет выглядеть следующим образом:
 AI2(SO4)3 + 3Na2S + 6H2O 3Na2SO4 + 2AI(OH)3↓ + 3H2S↑
AI2(SO4)3 + 3Na2S + 6H2O 3Na2SO4 + 2AI(OH)3↓ + 3H2S↑
Константы диссоциации некоторых слабых электролитов
в водных растворах при 250С
| Электролит | К | ||
| Азотистая кислота | HNO2 | 2,6 ∙10-5 | |
| Аммония гидроксид | NH4OH | 4 ∙10-4 | |
| Борная кислота | H3BO3 | K1 | 5,8 ∙10-4 |
| Бромноватистая кислота | HOBr | 2,1 ∙ 10-9 | |
| Водорода пероксид | H2O2 | K1 | 2,6 ∙10-12 |
| Кремниевая кислота | H2SiO3 | K1 K2 | 2,2 ∙10-10 1,6 ∙10-12 |
| Муравьиная кислота | HCOOH | 1,8 ∙10-4 | |
| Сернистая кислота | H2SO3 | K1 K2 | 1,6 ∙ 10-2 6,3 ∙10-8 |
| Сероводород | H2S | K1 K2 | 6 ∙10-8 1 ∙10-14 |
| Угольная кислота | H2CO3 | K1 K2 | 4,5 ∙10-7 4,7 ∙10-11 |
| Уксусная кислота | CH3COOH | 1,8 ∙10-5 | |
| Фосфорная кислота | H3PO4 | K1 K2 K3 | 7,5 ∙ 10-3 6,3 ∙10-8 1,3 ∙10-12 |
| Циановодород | HCN | 7,9 ∙10-10 | |
| Щавелевая кислота | H2C2O4 | K1 K2 | 5,4 ∙10-2 5,4 ∙10-5 |
Список рекомендуемой литературы
1. Карапетьянц М.Х., Дракин С.И.. Общая и неорганическая химия.- М.: Химия, 2001.- 632 с.
2. Зайцев О.С. Задачи и вопросы по химии.- М.: Химия, 1985.- 301 с.
3. Глинка Н.Л. Задачи и упражнения по общей химии.- Л.: Химия, 2004.- 270 с.
4. Гольбрайх З.Е. Сборник задач и упражнений по химии.- М.: Высшая школа, 2004.- 224 с.
Задание № 7
|
из
5.00
|
Обсуждение в статье: Задачи для самостоятельного решения. 5.1. Написать в ионно-молекулярной форме уравнения реакций |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

