 |
Главная |
Другие производные угольной кислоты
|
из
5.00
|
Иминомочевина (гуанидин) входит в состав аминокислоты аргинина:
H2N - C - NH2
NH
Н2N – СООН – карбаминовая кислотата – неполный амид угольной ки- слоты. В свободном состоянии не существует, однако соли (карбаматы) и эфи- ры (уретаны) этой кислоты достаточно устойчивы и находят практическое при- менение. Эфиры являются снотворными средствами
Содержание
1. Биологически важные одно- и многоатомные спирты, фенолы....................................................................................................... 3
1.1. Одноатомные спирты...................................................................... 5
1.2. Многоатомные спирты................................................................. 14
1.3. Фенолы........................................................................................... 19
1.4. Лабораторная работа “Свойства спиртов, фенлов”…..................................................................................... 29
2. Биологически важные амины..................................................... 32
3. Биологически важные карбонильные соединения: альдегиды и кетны....................................................................................................... 42
3.1. Лабораторная работа “Свойства альдегидов и кетонов”........ 58
4. Биологически важные карбоновые кислоты и их производные......... 61
4.1. Одноосновные карбоновые кислоты........................................... 67
4.2. Двухосновные карбоновые кислоты........................................... 72
4.3. Мочевина...................................................................................... 74
4.4. Другие производные угольной кислоты.................................... 77
4.5. Лабораторная работа “Свойства одно- и двухосновных карбо- новых кислот. Свойства мочевины”............................. 78
5. Тестовые задания для самостоятельной работы студентов................ 81
5.1. Тестовые задания по теме: Спирты. Фенолы............................. 81
5.2. Тестовые задания по теме: Амины.............................................. 83
5.3. Тестовые задания по теме: Альдегиды и кетоны........................ 84
5.4. Тестовые задания по теме: Карбоновые кислоты. Мочевина...................................................................................... 86
6. Эталоны ответов к тестовым заданиям................................................ 88
Используемая литература......................................................................... 89
“Гидрокси- и оксокислоты”
Цель занятия: изучение электронного, пространственного строения и хи- мических свойств биологически важных гидрокси- и оксокислот.
Студент должен знать:
- классификацию гидрокси- и оксокислот;
- номенклатуру и изомерию гидрокси- и оксокислот;
- особенности химических свойств оксо - , гидрокси - и фенолокислот;
Студент должен уметь:
- писать уравнения химических реакций оксо - , гидрокси - и фенолокислот;
- объяснять химическое поведение гидроксикислот в организме;
- объяснять кето - енольную таутомерию, роль этого фактора в биохимии организма.
Перечень вопросов для подготовки по теме “ Гидрокси- и оксокислоты ”
1. Гидроксикислоты (одноосновные (молочная), двухосновные (винные, яблочная) и трехосновные (лимонная) кислоты). Классификация. Номенк- латура. Изомерия. Химические свойства как гетерофункциональных соеди-

| -, |

| - |
 нений. Специфические реакции и -гидроксикислот алифатического
нений. Специфические реакции и -гидроксикислот алифатического
ряда. Лактоны, лактиды, их отношение к гидролизу.
2. Фенолокислоты. Салициловая кислота. Получение и химические свойства как гетерофункционального соединения. Эфиры салициловой ки- слоты, применяемые в медицине: метилсалицилат, фенилсалицилат, аце- тилсалициловая кислота, п-аминосалициловая кислота (ПАСК).
3. 
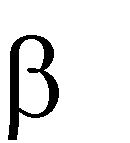 Оксокислоты (альдегидо- (глиоксиловая) и кетонокислоты (пировино- градная, ацетоуксусная, щавелевоуксусная, -кетоглутаровая)). Номенкла- тура. Изомерия. Химические свойства как гетерофункциональных соедине- ний. Специфические свойства в зависимости от взаимного расположения функциональных групп.
Оксокислоты (альдегидо- (глиоксиловая) и кетонокислоты (пировино- градная, ацетоуксусная, щавелевоуксусная, -кетоглутаровая)). Номенкла- тура. Изомерия. Химические свойства как гетерофункциональных соедине- ний. Специфические свойства в зависимости от взаимного расположения функциональных групп.
4. Кето-енольная таутомерия -оксокислот (ацетоуксусной и щавелево- уксусной).
Гидрокси(окси)кислоты
Это гетерофункциональные органические вещества, содержащие одно- временно одну или несколько гидроксильных (–ОН) и карбоксильных групп (–СООН). Количество карбоксильных групп (–СООН) определяет основ- ность, а гидроксильных ( –ОН) – атомность.
В общем виде их формулу можно представить
В простейшем случае n = m = 1.
Номенклатура.
R /(COOH)n .
\(OH)m
По международной номенклатуре ИЮПАК в составе молекулы выделяют функциональные группы и определяют их старшинство. Карбоксильная группа старше гидроксильной, следовательно, определяет окончание назва- ния, а младшая гидроксильная группа указывается приставкой гидрокси- или окси-. Родоначальная структура (главная цепь) выбирается так, чтобы в нее входило максимальное количество карбоксильных и затем гидроксильных групп. Нумерация цепи начинается от углеродного атома карбоксильной группы и ведется таким образом, чтобы сумма номеров всех заместителей была минимальной. В названии цифрами указывается положение всех замес- тителей и функциональных групп. Одинаковые заместители называют один раз, но с соответствующей цифровой приставкой: ди – 2, три -3, тетра- 4 и т.д.
Для оксикислот распространена радикально-функциональная номенклатура. Предварительно атомы углерода, следующие за карбоксильной группой ну- меруют буквами греческого алфавита. Основу названия составляет тривиаль- ное название соответствующей кислоты, а положение гидроксильных групп указывается приставкой гидрокси- или окси- и буквой греческого алфавита того углеродного атома с которым она связана.
Тривиальная(историческая) номенклатура оксикислот очень распространена.



 Таблица. Номенклатура гидроксикислот.
Таблица. Номенклатура гидроксикислот.
| Формула кислоты | Название по номенклатуре | ||
| ИЮПАК | радикально- заместитель- ной | триви- аль-ной | |
| CH2 COOH OH | 2-гидроксиэтановая | -окси- уксусная | гликоле- вая |
| H3C CH COOH OH | 2-гидрокси- пропановая | -окси- пропионовая | молочная |
| HOOC CH CH COOH OH OH | 2,3-дигидрокси- бутандиовая | , -диокси- янтарная | винная |
| COOH HOOC CH2 C CH2 COOH OH | 3-гидрокси- 3-карбокси- пентандиовая | - | лимонная |
 Изомерия.
Изомерия.
Для оксикислот характерна структурная и пространственная изомерия. Виды структурной изомерии:


 Изомерия положения гидроксильных групп
Изомерия положения гидроксильных групп
   H3C CH2 CH COOH
OH
H3C CH2 CH COOH
OH
|   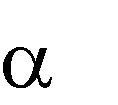 H3C CH CH2 COOH
OH
H3C CH CH2 COOH
OH
| H2C CH2 CH2 COOH OH |
| -оксимасляная кислота | -оксимасляная кислота | -оксимасляная кислота |



 Изомерия углеродного скелета
Изомерия углеродного скелета
| H3C CH2 CH COOH OH | CH3 H3C C COOH OH |
| -оксимасляная кислота | -оксиизомасляная кислота |
 Межклассовая изомерия
Межклассовая изомерия
Спирты изомерны простым эфирам, а карбоновые кислоты сложным эфирам. Можно привести примеры нескольких изомеров общей формулы С4Н8О3
| 4 3 2 1 O H3C CH2 CH C OH OH | 3 2 1 O CH3 CH C OH OCH3 | 3 2 1 O CH3 CH C OCH3 OH |
| 2-гидроксибутановая ки- слота | 2-метоксипропановая кислота | метиловый эфир пропановой кислоты |
Пространственная изомерия:
В ряду оксикарбоновых кислот важнейшим видом пространственной изомерии является оптическая изомерия. Она связана с наличием в молеку- лах одного или нескольких асимметрических(хиральных) атомов углерода. В ряду одноосновных двухатомных кислот атом углерода с четырьмя различ- ными заместителями (хиральный) появляется в молочной кислоте, следова- тельно, имеются оптические изомеры.
| COOH COOH H OH HO H CH3 CH3 | |
| D(–) – молочная кислота | L(+) – молочная кислота |
Буквами D,L- обозначают относительную конфигурацию оптических изомеров. Таким способом определяют строение ассиметрического атома по сравнению со строением стандартного вещества. Стандартом в ряду окси- кислот принимаются изомеры молочной кислоты. К D-ряду относится изо- мер, в котором гидроксогруппа в формуле Фишера расположена справа от главной цепи, к L-ряду - гидроксогруппа слева.
Оптические изомеры обладают свойством оптической активности (способность отклонять плоскость поляризации плоско поляризованного мо- нохроматического света на определенный угол). Один изомер отклоняет плоскость поляризации по часовой стрелке (вправо) - это правовращающий изомер, его обозначают знаком «+». Второй изомер – левовращающий, обо- значают знаком «–». Знак вращения плоскости поляризации света нельзя свя- зывать с отнесением соединений к D – и L – рядам, его определяют только экспериментально прибором - поляриметром.
Число оптических изомеров определяется по формуле : N = 2n, где N-
число оптических изомеров, n- число хиральных атомов углерода.
Винная кислота имеет два ассиметрических атома углерода, по форму- ле предсказывается наличие четырех оптических изомеров. Однако, изомеров существует только три: из них два оптически активных и один- неактивная мезоформа. Мезоформа появляется при наличии в молекуле двух одинаковых ассиметрических атомов, между которыми создается плоскость симметрии.
| COOH COOH COOH
H OH HO H H OH плоскость симметрии HO H H OH H OH
COOH COOH COOH | ||
| D(+) – винная кислота | L(–) – винная кислота | мезовинная кислота |
Для оксикислот с двумя ассиметрическими атомами углерода опреде- ление принадлежности к D,L – ряду затруднено. По договоренности опреде- ляют принадлежность D либо L – ряду по расположению заместителей у ближнего к старшей функциональной группе хирального атома в сравнении с веществом-стандартом.
 Химические свойства.
Химические свойства.
Наличие в молекуле двух типов функциональных групп приводит к тому, что эти соединения проявляют характерные свойства карбоновых кислот и одновременно спиртов. За счет взаимного влияния групп происходит уси- ление реакционной способности каждой из них. Кроме того, для оксикис- лот возможны специфические реакции с участием обеих групп.



 - I COOH O
- I COOH O
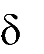

| O |
 H OH
H OH
- I OH
|
из
5.00
|
Обсуждение в статье: Другие производные угольной кислоты |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

