 |
Главная |
I. Реакции по карбоксильной группе.
|
из
5.00
|
 Кислотные свойства
Кислотные свойства
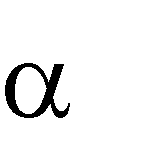
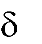


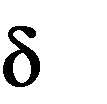


 Оксикислоты являются более сильными кислотами, чем соответствующие им карбоновые кислоты. Это объясняется акцепторным влиянием гидро- ксильной группы на карбоксильную. Например, -оксиуксусная кислотата (гликолевая) в 5 раз сильнее уксусной кислоты. Гидроксильная группа за счет отрицательного индуктивного эффекта притягивает к себе электрон- ную плотность ближайших углеродных атомов, тем самым увеличивает недостаток электронов на карбоксильном атоме углерода и облегчает дис- социацию группы ОН.
Оксикислоты являются более сильными кислотами, чем соответствующие им карбоновые кислоты. Это объясняется акцепторным влиянием гидро- ксильной группы на карбоксильную. Например, -оксиуксусная кислотата (гликолевая) в 5 раз сильнее уксусной кислоты. Гидроксильная группа за счет отрицательного индуктивного эффекта притягивает к себе электрон- ную плотность ближайших углеродных атомов, тем самым увеличивает недостаток электронов на карбоксильном атоме углерода и облегчает дис- социацию группы ОН.
| O O H3C C CH2 C 2 1 2 1 OH O H OH - Iэф , ЭА | |
| уксусная кислота | -оксиуксусная кислота |
Оксикислоты в растворах диссоциируют по карбоксильной группе:
| H3C CH COOH H3C CH COO + H OH OH | |
| молочная кислота | лактат-анион |
Соли образуются с активными металлами, основными оксидами, осно- ваниями, солями более слабых кислот:
недостаток
+ NaOH H3C CH COONa + H2O
H3C CH COOH OH
+ 2NaOH
избыток
OH
H3C CH COONa + 2H2O
ONa
S hvtHfJQH19zXfCWei+JyJqC7D/+2rqs7+sQFPjXgXIjXl5Dp6cd95jpNje3iQoBjuwFq7pzG0leD cQqMWC99DolPcXPrmA4M60r8U2z0mzgbNqs9vkdivdrQBQf60QoY+yDNV3tQYOXxd0VwFrz9Xgv6 Mgr7b16f/bdvvPkvAAAA//8DAFBLAwQUAAYACAAAACEA0OGBbOEAAAALAQAADwAAAGRycy9kb3du cmV2LnhtbEyPQUvDQBCF74L/YRnBm90kNUHSTEop6qkItoL0ts1Ok9DsbMhuk/Tfu570OG8e732v WM+mEyMNrrWMEC8iEMSV1S3XCF+Ht6cXEM4r1qqzTAg3crAu7+8KlWs78SeNe1+LEMIuVwiN930u pasaMsotbE8cfmc7GOXDOdRSD2oK4aaTSRRl0qiWQ0Ojeto2VF32V4PwPqlps4xfx93lvL0dD+nH 9y4mxMeHebMC4Wn2f2b4xQ/oUAamk72ydqJDSJ+zgO4RkiRLQARHFqVBOSEs4ygFWRby/4byBwAA //8DAFBLAQItABQABgAIAAAAIQC2gziS/gAAAOEBAAATAAAAAAAAAAAAAAAAAAAAAABbQ29udGVu dF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhADj9If/WAAAAlAEAAAsAAAAAAAAAAAAAAAAALwEA AF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAG19vw+kDAAAxUMAAA4AAAAAAAAAAAAAAAAALgIA AGRycy9lMm9Eb2MueG1sUEsBAi0AFAAGAAgAAAAhANDhgWzhAAAACwEAAA8AAAAAAAAAAAAAAAAA /g4AAGRycy9kb3ducmV2LnhtbFBLBQYAAAAABAAEAPMAAAAMEAAAAAA= "> 






 Кислотные свойства гидроксильной группы по сравнению с соответст- вующими спиртами усиливаются из-за акцепторного влияния карбоксильной группы.
Кислотные свойства гидроксильной группы по сравнению с соответст- вующими спиртами усиливаются из-за акцепторного влияния карбоксильной группы.
| O H3C CH2 H3C CH C OH O H - I OH эф , ЭА | |
| этанол | молочная кислота («кар- боксиэтанол») |
Вследствие чего с избытком основания соли образуются и по спирто- вой группе, что для одноатомных спиртов не характерно.
Двухосновные кислоты образуют два ряда солей - средние и кислые. Кислые соли, как правило, мало растворимы в воде, средние – хорошо рас- творимы. Это используют для обнаружения ионов калия в фармации и в ана- литической химии:
HOOC
CH CH COOH + KOH
KOOC
CH CH COOH
+ H2O
OH OH OH OH
гидротартрат калия
KOOC
CH CH COOH
+ KOH
KOOC
CH CH COOK
+ H2O
OH OH OH OH
гидротартрат калия тартрат калия
По тривиальной номенклатуре соли молочной кислоты называются лактаты, яблочной (2-гидроксибутандиовой) – малаты, лимонной – цитраты, винной – тартраты, смешанная калийно-натриевая соль винной кислоты на- зывается сегнетовой солью.
 Образование функциональных производных по карбоксильной груп- пе (реакции нуклеофильного замещения гидроксильной группы SN ОН)
Образование функциональных производных по карбоксильной груп- пе (реакции нуклеофильного замещения гидроксильной группы SN ОН)
Оксикислоты образуют все основные вилы функциональных производных карбоновых кислот.
Реакция с пентахлоридом фосфора идет сразу по двум функциональным группам. На хлор одновременно замещается и свободная спиртовая гидро- ксильная группа и связанная в составе карбоксильной.
| + CH3OH t0, H+ |
| + NH3 |
| + 2PCl5 |
H3C CH C
OH O
+ H2O CH3
метиловый эфир молочной кислоты
O O O
H3C CH C
H3C CH C
t0
 - H O H3C CH C
- H O H3C CH C
OH OH
OH ONH4 2
OH NH2
лактат аммония амид молочной кислоты
O
H C CH C + 2 HCl + 2 POCl
3 3
Cl Cl
хлорангидрид
2-хлорпропановой кислоты
|
из
5.00
|
Обсуждение в статье: I. Реакции по карбоксильной группе. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

